Transmisyjny mikroskop elektronowy – czym różnią się SEM, STM i TEM?
STM pojawił się w 1981 roku, kiedy szwajcarscy fizycy Gerd Binnig i Heinrich Rohrer postanowili zbudować narzędzie do badania lokalnego przewodnictwa powierzchni. Binnig i Rohrer wybrali powierzchnię złota na swój pierwszy obraz. Kiedy obraz był wyświetlany na ekranie monitora telewizyjnego, widzieli rzędy dokładnie rozmieszczonych atomów i obserwowali szerokie tarasy oddzielone stopniami o wysokości jednego atomu. Binnig i Rohrer odkryli w STM prostą metodę tworzenia bezpośredniego obrazu struktury atomowej powierzchni. Ich odkrycie otworzyło nową erę w nauce o powierzchni, a ich imponujące osiągnięcie zostało uhonorowane nagrodą Nobla w dziedzinie fizyki w 1986 roku.
Zasady działania
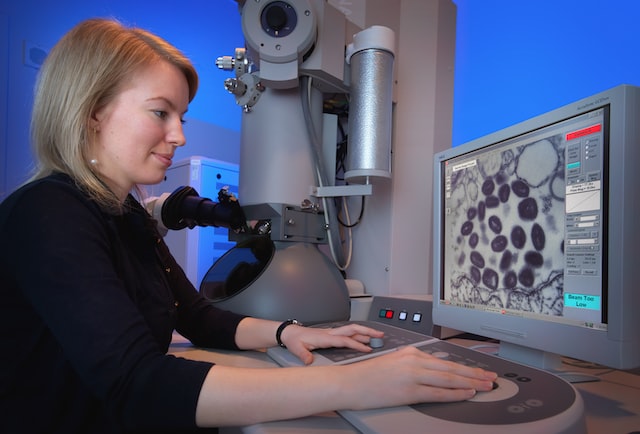
STM to mikroskop elektronowy o rozdzielczości wystarczającej do rozdzielenia pojedynczych atomów. Ostra końcówka w STM jest podobna do tej w skaningowym mikroskopie elektronowym (SEM), ale różnice między tymi dwoma instrumentami są głębokie. W SEM elektrony są wydobywane z końcówki za pomocą szeregu dodatnio naładowanych płytek umieszczonych kilka centymetrów za końcówką. Elektrony na wierzchołku końcówki są ograniczone do obszaru w metalu przez barierę potencjału. Siła przyciągania dodatniego ładunku na płytkach jest wystarczająca, aby elektrony mogły pokonać barierę i wejść do próżni jako swobodne cząstki. Otwory w dalszych płytkach tworzą soczewkę elektronową, która przekształca rozbieżną wiązkę z końcówki w wiązkę zbiegającą się w ognisku na powierzchni próbki.
Droga elektronu
W STM płytki tworzące soczewkę w SEM są usuwane, a końcówka jest umieszczana blisko próbki. Elektrony poruszają się przez barierę w sposób podobny do ruchu elektronów w metalu. W metalach elektrony wydają się być swobodnie poruszającymi się cząstkami, ale jest to iluzoryczne. W rzeczywistości elektrony przemieszczają się z atomu do atomu, przechodząc przez barierę potencjału między dwoma atomami.
W typowym przypadku, gdy atomy są oddalone od siebie o pięć angstremów, istnieje skończone prawdopodobieństwo, że elektron przeniknie przez barierę i przemieści się do sąsiedniego atomu. Elektrony poruszają się wokół jądra i zbliżają się do bariery z częstotliwością 1017 na sekundę. Przy każdym podejściu do bariery prawdopodobieństwo tunelowania wynosi 10−4, a elektrony przecinają barierę z szybkością 1013 na sekundę. Ta wysoka szybkość przenoszenia oznacza, że ruch jest zasadniczo ciągły, a tunelowanie można zignorować w metalach.